Бүгінгі таңда PRP деп аталатын тұжырымдама алғаш рет 1970 жылдары гематология саласында пайда болды.Гематологтар перифериялық қанның негізгі мәнінен жоғары тромбоциттер санынан алынған плазманы сипаттау үшін ондаған жылдар бұрын PRP терминін жасады.Он жылдан астам уақыттан кейін PRP жақ-бет хирургиясында тромбоциттерге бай фибриннің (ПҚФ) түрі ретінде қолданылды.Осы PRP туындысындағы фибриннің мазмұны оның жабысқақтығы мен тұрақты күй сипаттамаларына байланысты маңызды мәнге ие, ал PRP қабынуға қарсы қасиеттерге ие және жасуша пролиферациясын ынталандырады.Ақырында, шамамен 1990 жылдары PRP танымал бола бастады.Ақырында, бұл технология медицинаның басқа салаларына ауыстырылды.Содан бері позитивті биологияның бұл түрі кеңінен зерттеліп, кәсіби спортшылардың тірек-қимыл аппаратының әртүрлі жарақаттарын емдеуге қолданылды, бұл оның бұқаралық ақпарат құралдарында кеңінен таралуына одан әрі ықпал етті.ПРП ортопедия мен спорттық медицинада тиімді болумен қатар офтальмология, гинекология, урология және кардиология, педиатрия және пластикалық хирургияда да қолданылады.Соңғы жылдары PRP тері жараларын емдеуде, тыртықтарды қалпына келтіруде, тіндерді қалпына келтіруде, теріні жасартуда және тіпті шаш түсуде потенциалы үшін дерматологтар тарапынан жоғары бағаланды.
PRP емдеу және қабыну процестерін тікелей манипуляциялай алатынын ескере отырып, емдеу каскадын сілтеме ретінде енгізу қажет.Емдеу процесі келесі төрт кезеңге бөлінеді: гемостаз;Қабыну;Жасуша мен матрицалық пролиферация, соңында жараның қайта құрылуы.
Тіндерді емдеу
Тіндерді сауықтыру каскадты реакциясы белсендіріледі, бұл тромбоциттердің агрегациясына әкеледі тромбтардың пайда болуына және уақытша жасушадан тыс матрицаның (ECM) дамуына.Содан кейін тромбоциттер ашық коллаген мен ECM протеиніне жабысып, а-түйіршіктерінде бар биоактивті молекулалардың босатылуын тудырады.Тромбоциттерде өсу факторларын, химиотерапия факторларын және цитокиндерді, сондай-ақ простагландин, простата циклін, гистамин, тромбоксан, серотонин және брадикинин сияқты қабынуға қарсы медиаторларды қоса алғанда, әртүрлі биоактивті молекулалар бар.
Емдеу процесінің соңғы кезеңі жараның қайта құрылуына байланысты.Тіндердің қайта құрылуы анаболикалық және катаболикалық реакциялар арасындағы тепе-теңдікті орнату үшін қатаң түрде реттеледі.Бұл кезеңде тромбоциттерден алынатын өсу факторы (PDGF) және трансформациялық өсу факторы (TGF-β) Фибронектин және фибронектин фибробласттардың пролиферациясын және миграциясын, сондай-ақ ЭКМ компоненттерінің синтезін ынталандырады.Дегенмен, жараның жетілу уақыты көп дәрежеде жараның ауырлығына, жеке ерекшеліктеріне және зақымдалған тіннің ерекше емдік қабілетіне байланысты.Кейбір патофизиологиялық және метаболикалық факторлар тіндердің ишемиясы, гипоксия, инфекция, өсу факторларының теңгерімсіздігі және тіпті метаболикалық синдроммен байланысты аурулар сияқты емдеу процесіне әсер етуі мүмкін.
Қабынуға қарсы микроорта емдеу процесіне кедергі келтіреді.Ең қиыны, жоғары протеаза белсенділігі өсу факторының (GF) табиғи әсерін тежейді.Митоздық, ангиогендік және хемотактикалық қасиеттерден басқа, PRP көптеген өсу факторларының бай көзі болып табылады.Бұл биомолекулалар қабынудың жоғарылауын бақылау және анаболикалық ынталандыруды орнату арқылы қабыну тіндеріндегі зиянды әсерлерге қарсы тұра алады.Осы сипаттарды ескере отырып, зерттеушілер әртүрлі күрделі жарақаттарды емдеуде үлкен әлеуетті таба алады.
Көптеген аурулар, әсіресе тірек-қимыл аппаратының сипаты, остеоартритті емдеуге арналған PRP сияқты қабыну процесін реттейтін биологиялық өнімдерге қатты тәуелді.Бұл жағдайда артикулярлық шеміршектің денсаулығы анаболикалық және катаболикалық реакциялардың дәл балансына байланысты.Осы принципті ескере отырып, белгілі бір позитивті биологиялық агенттерді қолдану салауатты тепе-теңдікке жетуде табысты болуы мүмкін.PRP тромбоциттерді босатады, өйткені ол α- түйіршіктердегі өсу факторлары тіндердің трансформациясының әлеуетін реттеу үшін кеңінен қолданылады, бұл да ауырсынуды азайтады.Шын мәнінде, PRP емдеудің негізгі мақсаттарының бірі - негізгі қабыну және катаболикалық микроортаны тоқтату және қабынуға қарсы препараттарға трансформацияға ықпал ету.Басқа авторлар бұрын тромбинмен белсендірілген PRP бірнеше биологиялық молекулалардың шығарылуын арттыратынын көрсетті.Бұл факторларға гепатоциттердің өсу факторы (HGF) және ісік некрозының факторы (TNF- α) 、 Трансформациялаушы өсу факторы beta1 (TGF- β 1), тамырлы эндотелий өсу факторы (VEGF) және эпидермис өсу факторы (EGF) жатады.Басқа зерттеулер PRP 2 типті коллаген мен агрекан мРНҚ деңгейлерінің жоғарылауына ықпал ететінін көрсетті, сонымен бірге олардағы қабынуға қарсы цитокин интерлейкин – (IL) 1 тежелуін азайтады.Сондай-ақ, HGF және TNF- α [28] арқасында PRP қабынуға қарсы әсерді орнатуға көмектесуі мүмкін деп ұсынылды.Бұл молекулалық препараттардың екеуі де kappaB (NF- κВ) ядролық факторын белсендіруге қарсы белсенділік пен экспрессияны төмендетеді;Екіншіден, TGF-β 1 экспрессиясы арқылы моноциттердің хемотаксисінің алдын алады, осылайша TNF-α әсері химокиндердің трансактивациясына қарсы әрекет етеді.HGF PRP арқылы туындаған қабынуға қарсы әсерде таптырмас рөл атқарады.Бұл күшті қабынуға қарсы цитокин NF-κ B сигналдық жолын бұзады және қабынуға қарсы цитокин экспрессиясы қабыну реакциясын тежейді.Сонымен қатар, PRP азот оксидінің (NO) жоғары деңгейін төмендете алады.Мысалы, артикулярлы шеміршектерде NO концентрациясының жоғарылауы коллаген синтезін тежейтіні және хондроцит апоптозын индукциялайтыны дәлелденген, сонымен бірге матрицалық металлопротеиназалардың (ММП) синтезін жоғарылатады, осылайша катаболизмнің өзгеруіне ықпал етеді.Жасуша дегенерациясы тұрғысынан PRP сонымен қатар белгілі бір жасуша түрлерінің аутофагиясын басқаруға қабілетті болып саналады.Соңғы қартаю күйіне жеткенде кейбір жасуша топтары статикалық күй мен өзін-өзі жаңарту мүмкіндігін жоғалтады.Дегенмен, соңғы зерттеулер PRP емдеу бұл зиянды жағдайларды жақсы қалпына келтіре алатынын көрсетті.Мусса және оның әріптестері PRP адам остеоартритінің шеміршек апоптозын азайта отырып, аутофагия мен қабынуға қарсы маркерлерді жоғарылату арқылы хондроциттерді қорғауды тудыруы мүмкін екенін дәлелдеді.Гарсиа Пратт және т.б.Аутофагия бұлшықет дің жасушаларының демалу және қартаю тағдыры арасындағы ауысуды анықтайды деп хабарлайды.Зерттеушілер in vivo, интеграцияланған аутофагияны қалыпқа келтіру жасушаішілік зақымданудың жиналуын болдырмайды және спутниктік жасушалардың қартаюына және функционалдық төмендеуіне жол бермейді деп санайды.Жақында Парриш пен Родес сияқты адамның бағаналы жасушаларының қартаюында да PRP қабынуға қарсы әлеуетін одан әрі ашып көрсетуге елеулі үлес қосты.Бұл жолы тромбоциттер мен нейтрофилдердің өзара әрекеттесуіне назар аударылады.Зерттеу барысында зерттеушілер арахидон қышқылы шығаратын белсендірілген тромбоциттер нейтрофилдермен сіңіп, белгілі қабыну молекулалары болып табылатын лейкотриендер мен простагландиндерге айналады деп түсіндірді.Дегенмен, тромбоциттердің нейтрофилдермен өзара әрекеттесуі лейкотриенді липопротеиндерге айналдыруға мүмкіндік береді, олар нейтрофилдердің белсендірілуін шектейтін және диализді болдырмайтын тиімді қабынуға қарсы ақуыз екендігі дәлелденген және емдік каскадтың соңғы сатысына дейін тұқым қуалауға ықпал етеді.
Қабынуға қарсы микроорта емдеу процесіне кедергі келтіреді.Ең қиыны, жоғары протеаза белсенділігі өсу факторының (GF) табиғи әсерін тежейді.Митоздық, ангиогендік және хемотактикалық қасиеттерден басқа, PRP көптеген өсу факторларының бай көзі болып табылады.Бұл биомолекулалар қабынудың жоғарылауын бақылау және анаболикалық ынталандыруды орнату арқылы қабыну тіндеріндегі зиянды әсерлерге қарсы тұра алады.
Жасуша факторы
PRP құрамындағы цитокиндер тіндерді қалпына келтіру процесін манипуляциялауда және қабыну зақымдануын реттеуде маңызды рөл атқарады.Қабынуға қарсы цитокиндер – негізінен белсендірілген макрофагтармен индукцияланған қабынуға қарсы цитокиндердің жауабын қамтамасыз ететін биохимиялық молекулалардың кең ауқымы.Қабынуға қарсы цитокиндер қабынуды реттеу үшін арнайы цитокин ингибиторларымен және еритін цитокиндік рецепторлармен әрекеттеседі.Интерлейкин (ИЛ) – 1 рецептор антагонистері, ИЛ-4, ИЛ-10, ИЛ-11 және ИЛ-13 негізгі қабынуға қарсы препараттар, цитокиндер ретінде жіктеледі.Әр түрлі жара түрлеріне сәйкес кейбір цитокиндер, мысалы, интерферон, лейкозды тежеу факторы, TGF-β және IL-6, олар қабынуға қарсы немесе қабынуға қарсы әсер көрсете алады.TNF-α、 IL-1 және IL-18 басқа ақуыздардың қабынуға қарсы әсерін тежей алатын белгілі цитокиндік рецепторларға ие [37].IL-10 - IL-1, IL-6 және TNF-α сияқты қабынуға қарсы цитокиндерді төмендететін және қабынуға қарсы факторларды жоғары реттейтін ең тиімді қабынуға қарсы цитокиндердің бірі.Бұл реттеуге қарсы механизмдер қабынуға қарсы цитокиндердің өндірісі мен қызметінде шешуші рөл атқарады.Сонымен қатар, белгілі бір цитокиндер тіндерді қалпына келтіру үшін маңызды болып табылатын фибробласттарды ынталандыру үшін арнайы сигналдық жауаптарды тудыруы мүмкін.Қабыну цитокині TGF β 1, IL-1 β, IL-6, IL-13 және IL-33 фибробласттарды миофибробласттарға дифференциациялау және ЭКМ жақсарту үшін ынталандырады [38].Өз кезегінде, фибробласттар TGF- β, IL-1 β, IL-33, CXC және CC цитокиндерін шығарады, макрофагтар сияқты иммундық жасушаларды белсендіру және тарту арқылы қабыну реакциясын ынталандырады.Бұл қабыну жасушалары жарада бірнеше рөл атқарады, негізінен жараны тазартуға және жаңа тіндерді қалпына келтіру үшін маңызды болып табылатын хемокиндердің, метаболиттер мен өсу факторларының биосинтезіне ықпал ету арқылы.Сондықтан PRP құрамындағы цитокиндер жасушалық типті иммундық жауапты ынталандыруда және қабыну кезеңінің регрессиясына ықпал етуде маңызды рөл атқарады.Шындығында, кейбір зерттеушілер бұл процесті «қалпына келтіретін қабыну» деп атады, бұл қабыну кезеңі, науқастың алаңдаушылығына қарамастан, қабыну сигналдарын беретін эпигенетикалық механизмді ескере отырып, тіндерді қалпына келтіру үдерісін сәтті аяқтау үшін қажетті және маңызды қадам болып табылады. жасуша пластикасын ынталандырады.
Ұрық терісінің қабынуындағы цитокиндердің рөлі регенеративті медицинаны зерттеу үшін үлкен маңызға ие.Ұрықтың және ересектердің сауығу механизмдерінің айырмашылығы - зақымдалған ұрық тіндері кейде ұрықтың жасына және сәйкес тіндердің түрлеріне сәйкес бастапқы күйіне оралады.Адамдарда ұрықтың терісі 24 апта ішінде толық қалпына келуі мүмкін, ал ересектерде жараның жазылуы тыртықтардың пайда болуына әкелуі мүмкін.Белгілі болғандай, сау тіндермен салыстырғанда, тыртық тіндерінің механикалық қасиеттері айтарлықтай төмендейді, ал олардың функциялары шектеулі.ИЛ-10 цитокиніне ерекше назар аударылады, ол амниотикалық сұйықтықта және ұрық терісінде жоғары экспрессияға ие және цитокиннің плейотропты әсерімен ықпал ететін ұрық терісін тыртықсыз қалпына келтіруде рөл атқаратыны дәлелденді.ZgheibC және т.б.Ұрық терісін трансгенді нокаут (КО) IL-10 тышқандарына және бақылау тышқандарына трансплантациялау зерттелді.IL-10KO тышқандары трансплантаттардың айналасында қабыну және тыртық түзілу белгілерін көрсетті, ал бақылау тобындағы трансплантаттарда биомеханикалық қасиеттерде айтарлықтай өзгерістер және тыртықтардың жазылуы байқалмады.
Қабынуға қарсы және қабынуға қарсы цитокиндердің экспрессиясы арасындағы нәзік тепе-теңдікті реттеудің маңыздылығы мынада, соңғысы артық өндірілген кезде, сайып келгенде, белгілі бір гендердің экспрессиясын азайту арқылы жасуша деградациясының сигналдарын жібереді.Мысалы, тірек-қимыл аппаратының медицинасында IL-1 β Down шеміршек дамуына жауап беретін SOX9-ды реттейді.SOX9 шеміршек дамуы үшін маңызды транскрипция факторларын шығарады, II типті коллаген альфа 1 (Col2A1) реттейді және II типті коллаген гендерін кодтауға жауап береді.IL-1 β Соңында Col2A1 және агрекан экспрессиясы төмендеді.Дегенмен, тромбоциттерге бай өнімдермен емдеу IL-1 β-ны тежейтіні көрсетілді, бұл әлі де коллагенді кодтайтын гендердің экспрессиясын сақтау және қабынуға қарсы цитокиндермен индукцияланған хондроциттердің апоптозын азайту үшін регенеративті медицинаның мүмкін серіктесі болып табылады.
Анаболикалық ынталандыру: Зақымдалған тіннің қабыну күйін реттеуден басқа, PRP құрамындағы цитокиндер митоз, химиялық тартылыс және пролиферация рөлдерін ойнай отырып, анаболикалық реакцияға қатысады.Бұл Cavallo және басқалары басқаратын in vitro зерттеуі.Адамның хондроциттеріне әртүрлі PRP әсерін зерттеу.Зерттеушілер салыстырмалы түрде төмен тромбоциттер мен лейкоциттердің концентрациясы бар PRP өнімдерінің қалыпты хондроцит белсенділігін ынталандыратынын байқады, бұл анаболикалық реакцияның кейбір жасушалық механизмдерін ынталандыруға қолайлы.Мысалы, ii типті коллаген мен агрегациялық гликандардың экспрессиясы байқалды.Керісінше, тромбоциттер мен лейкоциттердің жоғары концентрациясы әртүрлі цитокиндерді қамтитын басқа жасушалық сигналдық жолдарды ынталандыратын сияқты.Авторлар бұл нақты PRP формуласында лейкоциттердің көп болуына байланысты болуы мүмкін деп болжайды.Бұл жасушалар VEGF, FGF-b және интерлейкиндер IL-1b және IL-6 сияқты белгілі бір өсу факторларының экспрессиясының жоғарылауына жауапты болып көрінеді, бұл өз кезегінде TIMP-1 және IL-10-ды ынталандыруы мүмкін.Басқаша айтқанда, «жаман» PRP формуласымен салыстырғанда, тромбоциттер мен лейкоциттерге бай PRP қоспасы хондроциттердің салыстырмалы инвазивтілігіне ықпал ететін сияқты.
Schnabel және т.б. әзірлеген зерттеу.жылқы сіңір ұлпасындағы аутологиялық биоматериалдардың рөлін бағалауға арналған.Авторлар алты жас ересек жылқыдан (2-4 жас) қан мен сіңір үлгілерін жинады және құрамында PRP бар ортада өсірілген жылқылардың flexor digitorum superficialis сіңір экспланттарының гендік экспрессия үлгісін, ДНҚ және коллаген мазмұнын зерттеуге назар аударды. немесе басқа қан өнімдері.Сіңір экспланттары қанда, плазмада, PRP, тромбоциттер тапшылығы бар плазмада (PPP) немесе сүйек кемігінің аспираттарында (BMA) өсірілді және аминқышқылдары 100%, 50% немесе 10% сарысусыз DMEM қосылды.Қолданылатын биохимиялық талдауды… кейін жүргізу кезінде зерттеушілер TGF-β PRP ортасындағы PDGF-BB және PDGF-1 концентрациясы сыналған барлық басқа қан өнімдеріне қарағанда әсіресе жоғары екенін атап өтті.Сонымен қатар, 100% PRP ортасында өсірілген сіңір тіндері COL1A1, COL3A1 және COMP матрицалық белоктарының гендік экспрессиясының жоғарылауын көрсетті, бірақ MMPs3 және 13 катаболикалық ферменттерін арттырмады. Кем дегенде сіңір құрылымы тұрғысынан бұл in vivo зерттеу пайдалануды қолдайды. autolo – ірі сүтқоректілердің тендиниттерін емдеуге арналған подагра қанының өнімі немесе PRP.
Чен және т.б.PRP реконструкциялық әсері одан әрі талқыланды.Алдыңғы зерттеулер сериясында зерттеушілер шеміршек түзілуін күшейтумен қатар, PRP сонымен қатар ECM синтезінің жоғарылауына ықпал ететінін және артикулярлық шеміршек пен ядро пульпозының қабыну реакциясын тежейтінін дәлелдеді.PRP Smad2/3-β фосфорлануы арқылы TGF белсендіреді. Сигнал жолы жасушаның өсуі мен дифференциациясында маңызды рөл атқарады.Сонымен қатар, PRP белсендірілгеннен кейін пайда болған фибрин тромбтары жасушалардың жабысуына мүмкіндік беретін қатты үш өлшемді құрылымды қамтамасыз етеді, бұл жаңа тіндердің құрылысына әкелуі мүмкін деп саналады.
Басқа зерттеушілер дерматология саласындағы созылмалы тері жараларын емдеуге елеулі үлес қосты.Бұл да назар аударарлық.Мысалы, 2019 жылы Хеслер мен Шям жүргізген зерттеулер PRP мүмкін және тиімді балама ем ретінде құнды екенін көрсетеді, ал дәріге төзімді созылмалы ойық жара әлі де денсаулық сақтау саласына айтарлықтай экономикалық ауыртпалық әкеледі.Атап айтқанда, қант диабеті аяқтың жарасы - аяқ-қолдарды ампутациялауды жеңілдететін белгілі денсаулық сақтау проблемасы.Ахмед және басқалары жариялаған зерттеу.2017 жылы аутологиялық PRP гелі созылмалы қант диабеті аяқ жарасы бар науқастарда қажетті өсу факторларын шығару арқылы жараның жазылуын ынталандыруы мүмкін екенін көрсетті, осылайша емдеу жылдамдығын айтарлықтай жақсартады.Сол сияқты, Гончар мен оның әріптестері қант диабеті аяқ жараларын емдеуді жақсартудағы PRP және өсу факторы коктейльдерінің қалпына келтіру мүмкіндігін қарастырып, талқылады.Зерттеушілер өсу факторы қоспаларын пайдалану PRP және жалғыз өсу факторын қолданудың артықшылықтарын жақсарта алатын ықтимал шешім болуы мүмкін деп ұсынды.Сондықтан, жалғыз өсу факторын қолданумен салыстырғанда, PRP және басқа емдеу стратегияларының комбинациясы созылмалы ойық жараларды емдеуге айтарлықтай ықпал етуі мүмкін.
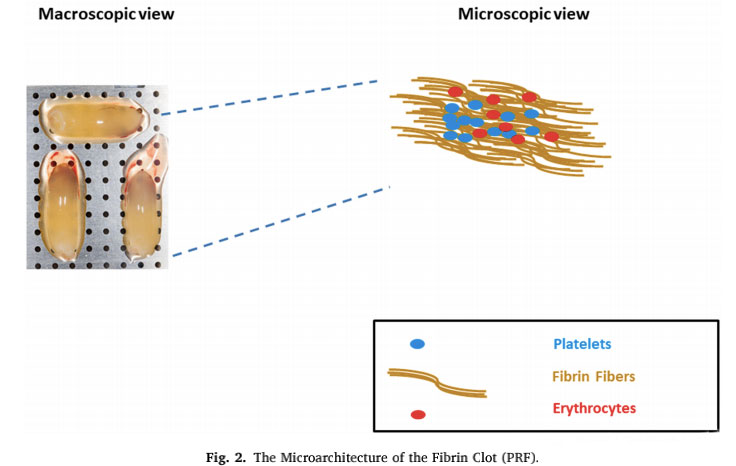
Фибрин
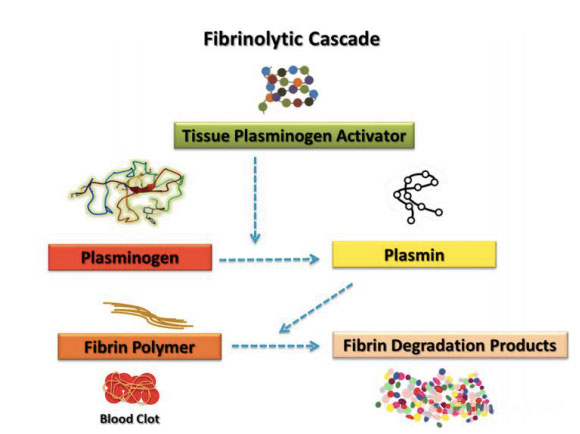
Тромбоциттер фибринолитикалық жүйеге қатысты бірнеше факторларды қамтиды, олар фибринолитикалық реакцияны жоғары немесе төмен реттей алады.Қан ұйығыштарының деградациясындағы гематологиялық компоненттер мен тромбоциттер функциясының уақыт арақатынасы мен салыстырмалы үлесі әлі де қоғамда кеңінен талқылауға тұрарлық мәселе болып табылады.Әдебиеттер емдеу процесіне әсер ету қабілетімен танымал тромбоциттерге ғана бағытталған көптеген зерттеулерді ұсынады.Көптеген көрнекті зерттеулерге қарамастан, коагуляция факторлары және фибринолитикалық жүйелер сияқты басқа гематологиялық компоненттер де жараларды тиімді қалпына келтіруге айтарлықтай үлес қосатыны анықталды.Анықтау бойынша фибринолиз фибриннің ыдырауына ықпал ететін белгілі бір ферменттердің белсендірілуіне байланысты күрделі биологиялық процесс болып табылады.Фибринолиз реакциясын басқа авторлар фибриннің ыдырау өнімдері (fdp) шын мәнінде тіндерді қалпына келтіруді ынталандыруға жауапты молекулалық агенттер болуы мүмкін деп ұсынды.Бұрынғы маңызды биологиялық оқиғалардың тізбегі фибриннің тұндыруынан және жараның жазылуына қажетті ангиогенезді жоюдан тұрады.Жарақаттан кейін тромбтардың пайда болуы тіндерді қан жоғалтудан және микробтық агенттердің инвазиясынан қорғау үшін қорғаныс қабаты ретінде қызмет етеді, сонымен қатар қалпына келтіру процесі кезінде жасушалар миграциялай алатын уақытша матрицаны қамтамасыз етеді.Қанның ұюы фибриногеннің сериндік протеаза арқылы ыдырауына байланысты, ал тромбоциттер өзара байланысқан фибриндік талшық торында жиналады.Бұл реакция қан ұйығыштарының пайда болуының негізгі оқиғасы болып табылатын фибрин мономерінің полимерленуін тудырды.Қан ұйығышын белсендірілген тромбоциттердің дегрануляциясы кезінде бөлінетін цитокиндер мен өсу факторларының резервуары ретінде де пайдалануға болады.Фибринолитикалық жүйе плазминмен қатаң реттеледі және жасуша миграциясын, өсу факторларының биожетімділігін және тіндердің қабынуы мен регенерациясына қатысатын басқа протеазалық жүйелерді реттеуде маңызды рөл атқарады.Урокиназа плазминоген активаторының рецепторы (uPAR) және плазминоген активаторының ингибиторы-1 (PAI-1) сияқты фибринолиздің негізгі компоненттері жараның сәтті жазылуы үшін қажетті арнайы жасуша түрлері болып табылатын мезенхималық дің жасушаларында (MSCs) экспрессияланатыны белгілі. .
Жасуша миграциясы
uPA uPAR ассоциациясы арқылы плазминогенді белсендіру - бұл жасушадан тыс протеолизді күшейтетіндіктен қабыну жасушаларының миграциясына ықпал ететін процесс.Трансмембраналық және жасушаішілік домендердің болмауына байланысты uPAR жасуша миграциясын реттеу үшін интегрин және вителлин сияқты рецепторларға мұқтаж.Бұдан әрі ол uPA uPAR байланысуы жасушалардың адгезиясына ықпал ететін витректонектин мен интегринге uPAR аффинділігінің жоғарылауына әкелетінін көрсетті.Плазминоген активаторының ингибиторы-1 (PAI-1) өз кезегінде жасушаларды ажыратады.Ол жасуша бетіндегі uPA upar integrin комплексінің uPA-мен байланысқанда, ол upar vitellin және integrin vitellin арасындағы өзара әрекеттесуді бұзады.
Регенеративті медицина аясында сүйек кемігінің мезенхималық дің жасушалары мүшелердің ауыр зақымдануы кезінде сүйек кемігінен жұмылдырылады, сондықтан олар көптеген сынықтары бар науқастардың қан айналымынан табылуы мүмкін.Алайда, нақты жағдайларда, мысалы, соңғы сатыдағы бүйрек жеткіліксіздігі, соңғы сатыдағы бауыр жеткіліксіздігі немесе жүрек трансплантациясынан кейін қабылдамау кезінде бұл жасушалар қанда анықталмауы мүмкін [66].Бір қызығы, бұл адамның сүйек кемігінен алынған мезенхималық (стромальды) тегі сау адамдардың қанында анықталмады [67].Сүйек кемігінің мезенхималық дің жасушаларын (BMSC) жұмылдырудағы uPAR рөлі бұрын ұсынылған, бұл гемопоэтикалық дің жасушаларының (HSC) мобилизациясында uPAR пайда болуына ұқсас.Варабанени және т.б.Нәтижелер uPAR тапшылығы бар тышқандарда гранулоциттердің колониясын ынталандыратын факторды қолдану MSC сәтсіздігін тудырғанын көрсетті, бұл жасуша миграциясында фибринолиз жүйесінің қолдаушы рөлін тағы бір рет күшейтті.Кейінгі зерттеулер сонымен бірге гликозилфосфатидилинозитпен бекітілген uPA рецепторлары белгілі бір жасушаішілік сигналдық жолдарды белсендіру арқылы адгезияны, миграцияны, пролиферацияны және дифференциацияны реттейтінін көрсетті: тірі фосфатидилинозитол 4,5-дифосфатты және 3-киназа/кинеза/3-киназа/2 сигналдық жолын белсендіру. (FAK).
MSC жарасын емдеу контекстінде фибринолитикалық фактор өзінің одан әрі маңыздылығын дәлелдеді.Мысалы, плазминоген тапшылығы бар тышқандар жараларды емдеу оқиғаларының қатты кешігуін көрсетті, бұл плазминнің бұл процесте маңызды екенін көрсетеді.Адамдарда плазминнің жоғалуы жараның жазылуының асқынуына әкелуі мүмкін.Қан ағымының үзілуі тіндердің регенерациясын айтарлықтай тежей алады, бұл сонымен қатар қант диабетімен ауыратын науқастарда бұл регенерация процестерінің неге қиынырақ екенін түсіндіреді.
Жараның жазылуын тездету үшін жара орнына сүйек кемігінің мезенхималық дің жасушалары тартылды.Тұрақты жағдайларда бұл жасушалар uPAuPAR және PAI-1 экспрессиясын көрсетті.Соңғы екі ақуыз гипоксияны индукциялайтын факторлар α (HIF-1 α) Мақсатты анықтау өте ыңғайлы, себебі MSC-дегі HIF-1 α FGF-2 және HGF белсендіру FGF-2 және HGF жоғары реттелуіне ықпал етті;HIF-2 α Өз кезегінде VEGF-A [77] жоғары реттеледі, ол бірге жараның жазылуына ықпал етеді.Сонымен қатар, HGF сүйек кемігінің мезенхималық дің жасушаларын жараланған жерлерге синергетикалық түрде тартуды күшейтетін сияқты.Ишемиялық және гипоксиялық жағдайлар жараларды қалпына келтіруге айтарлықтай кедергі келтіретінін атап өткен жөн.BMSC оттегінің төмен деңгейін қамтамасыз ететін тіндерде өмір сүруге бейім болғанымен, трансплантацияланған BMSCs in vivo өмір сүруі шектеледі, өйткені трансплантацияланған жасушалар көбінесе зақымдалған тіндерде байқалатын қолайсыз жағдайларда өледі.Гипоксия кезінде сүйек кемігінің мезенхималық дің жасушаларының адгезиясы және өмір сүру тағдыры осы жасушалардан бөлінетін фибринолитикалық факторларға байланысты.PAI-1 вителлинге жоғары жақындығы бар, сондықтан ол uPAR және интегриннің вителлинмен байланысуы үшін бәсекелесе алады, осылайша жасуша адгезиясы мен миграциясын тежейді.
Моноциттер және регенерация жүйесі
Әдебиеттерге сәйкес, жараларды емдеудегі моноциттердің рөлі туралы көптеген талқылаулар бар.Макрофагтар негізінен қан моноциттерінен шығады және регенеративті медицинада маңызды рөл атқарады [81].Нейтрофилдер IL-4, IL-1, IL-6 және TNF-α бөлетіндіктен, бұл жасушалар әдетте жарақаттан кейін шамамен 24-48 сағаттан кейін жараға енеді.Тромбоциттер тромбинді және тромбоциттік фактор 4 (PF4) шығарады, олар моноциттердің жиналуына ықпал етеді және макрофагтар мен дендритті жасушаларға дифференциацияланады.Макрофагтардың маңызды ерекшелігі олардың пластикалық қасиеті болып табылады, яғни олар фенотиптерді түрлендіре алады және басқа жасуша түрлеріне, мысалы, эндотелий жасушаларына дифференцияланады, содан кейін жара микроортасында әртүрлі биохимиялық тітіркендіргіштерге әртүрлі қызметтерді көрсетеді.Қабыну жасушалары ынталандыру көзі ретінде жергілікті молекулалық сигналға байланысты M1 немесе M2 екі негізгі фенотипті көрсетеді.M1 макрофагтары микробтық агенттермен индукцияланады, сондықтан олардың қабынуға қарсы әсері көбірек.Керісінше, M2 макрофагтары әдетте 2 типті реакциялар арқылы өндіріледі және әдетте IL-4, IL-5, IL-9 және IL-13 жоғарылауымен сипатталатын қабынуға қарсы қасиеттерге ие.Ол сонымен қатар өсу факторларын өндіру арқылы тіндерді қалпына келтіруге қатысады.M1-ден M2 қосалқы түріне көшу негізінен жараның жазылуының кеш кезеңімен байланысты.M1 макрофагтары нейтрофильді апоптозды қоздырады және осы жасушалардың клиренсін бастайды).Нейтрофилдердің фагоцитозы цитокиндердің өндірісі тоқтатылатын, макрофагтарды поляризациялайтын және TGF-β 1 шығаратын бірқатар оқиғаларды белсендіреді. емдік каскадта пролиферация фазасының басталуы [57].Жасушалық процестерге қатысатын тағы бір жоғары байланысты ақуыз - серин (SG).Бұл гемопоэтикалық жасушаның секреторлы түйіршігі протеогликаны секреторлық ақуыздарды мастикалық жасушалар, нейтрофилдер және цитотоксикалық Т лимфоциттер сияқты арнайы иммундық жасушаларда сақтау үшін қажет екендігі анықталды.Көптеген гемопоэтикалық емес жасушалар плазминогенді синтездесе де, барлық қабыну жасушалары бұл ақуыздың көп мөлшерін өндіреді және оны басқа қабыну медиаторларымен, соның ішінде протеазалармен, цитокиндермен, хемокиндермен және өсу факторларымен әрі қарай әрекеттесу үшін түйіршіктерде сақтайды.SG-дегі теріс зарядталған гликозаминогликан (GAG) тізбектері секреторлық түйіршіктердің тұрақтылығы үшін маңызды болып көрінеді, өйткені олар маңызды зарядталған түйіршікті компоненттерді жасушада, ақуызда және GAG тізбегінде спецификалық түрде байланыстырады және олардың сақталуын жеңілдетеді.PRP зерттеулеріне қатысуға қатысты, Вульф және әріптестері бұрын SG тапшылығы тромбоциттердің морфологиялық өзгерістерімен тығыз байланысты екенін көрсетті;Тромбоцит факторы 4 β- Тромбоглобулинде және тромбоциттерде PDGF сақтау ақаулары;Тромбоциттер агрегациясының және секрециясының нашарлығы in vitro және тромбоз ақауы in vivo.Сондықтан зерттеушілер бұл протеогликан тромбоздың негізгі реттеушісі болып көрінеді деген қорытындыға келді.
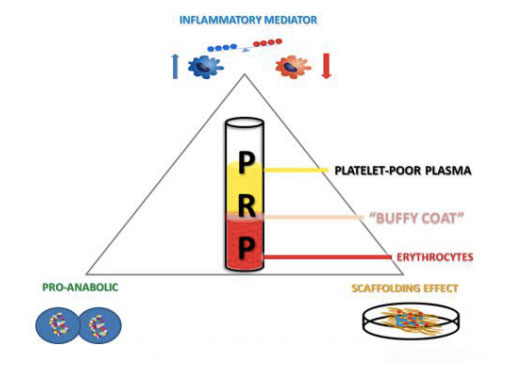
Тромбоциттерге бай өнімдер жеке қанды жинау және центрифугалау арқылы алуға және қоспаны плазма, тромбоциттер, ақ қан жасушалары және ақ қан жасушалары бар әртүрлі қабаттарға бөлуге болады.Тромбоциттер концентрациясы негізгі мәннен жоғары болғанда, ол ең аз жанама әсерлермен сүйек пен жұмсақ тіндердің өсуін жеделдетуі мүмкін.Аутологиялық PRP өнімдерін қолдану салыстырмалы түрде жаңа биотехнология болып табылады, ол әртүрлі тіндердің жарақаттарын емдеуді ынталандыруда және жақсартуда үнемі оптимистік нәтижелер көрсетті.Бұл балама емдеу әдісінің тиімділігі жараның физиологиялық жазылуын және тіндерді қалпына келтіру процесін имитациялау және қолдау үшін өсу факторлары мен ақуыздардың кең ауқымын жергілікті жеткізумен байланысты болуы мүмкін.Сонымен қатар, фибринолитикалық жүйе тіндердің қалпына келуіне маңызды әсер ететіні анық.Қабыну жасушаларының және сүйек кемігінің мезенхималық дің жасушаларының жасушалық жинақталуын өзгертуден басқа, ол жараларды емдеу аймақтарының протеолитикалық белсенділігін және сүйек, шеміршек және бұлшықетті қоса, мезодермальды тіндердің регенерация процесін реттей алады, сондықтан ол сүйек, шеміршек және бұлшықеттердің негізгі құрамдас бөлігі болып табылады. тірек-қимыл аппаратының медицинасы.
Жедел емдеу - бұл медицина саласындағы көптеген мамандардың алға қойған мақсаты.PRP оң биологиялық құрал болып табылады, ол регенеративті оқиғалар каскадын ынталандыру және үйлестіруде перспективалық дамуды қамтамасыз етуді жалғастыруда.Дегенмен, бұл терапевтік құрал әлі де өте күрделі болғандықтан, әсіресе сансыз биоактивті факторларды және олардың әртүрлі өзара әрекеттесу механизмдерін және сигнал беру әсерлерін шығаратындықтан, қосымша зерттеулер қажет.
(Осы мақаланың мазмұны қайта басылған және біз осы мақаладағы мазмұнның дәлдігіне, сенімділігіне немесе толықтығына ешқандай тікелей немесе жанама кепілдік бермейміз және осы мақаланың пікірлері үшін жауапты емеспіз, түсініңіз.)
Жіберу уақыты: 16 желтоқсан 2022 ж